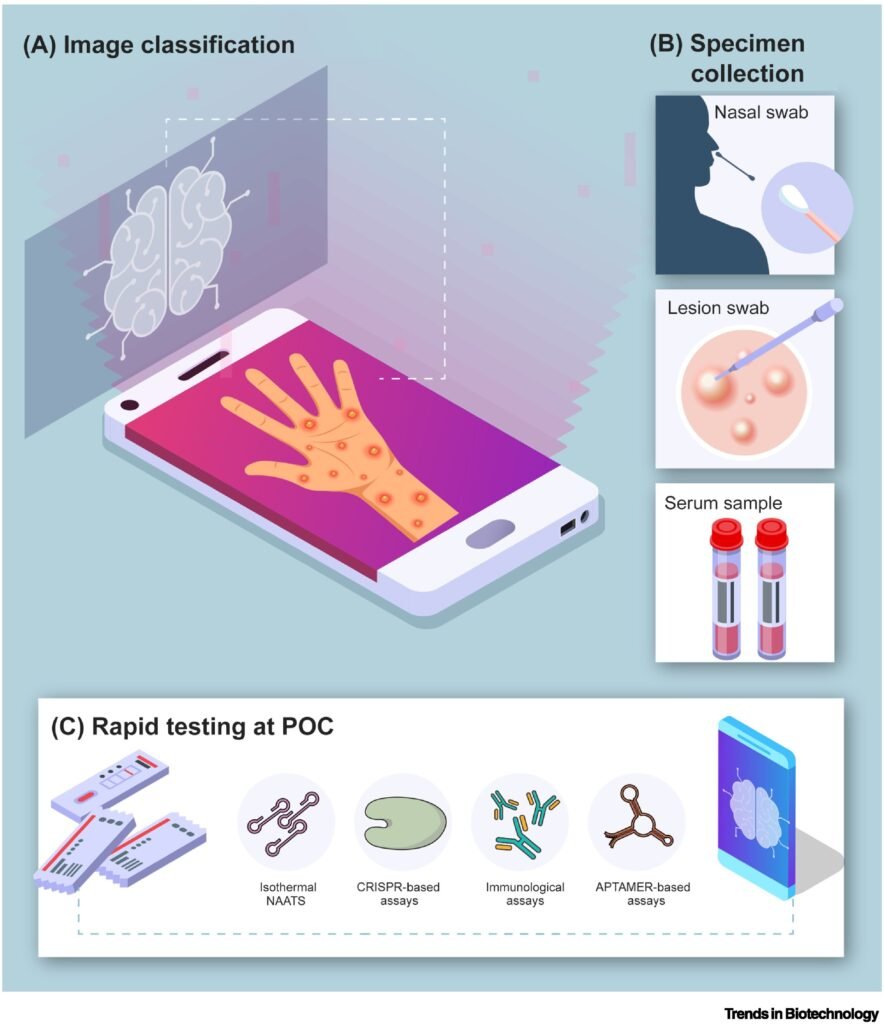
Nach dem Anstieg der Affenpockenfälle, insbesondere in Ländern, in denen die Krankheit bisher nicht vorkam, rief die Weltgesundheitsorganisation (WHO) im Juni 2022 und erneut im August 2024 einen internationalen Gesundheitsnotstand aus. Eine genaue und zeitnahe Diagnose ist entscheidend für die Eindämmung der Infektion. PCR-basierte Methoden – der Goldstandard für die Affenpockendiagnostik – erfordern jedoch eine komplexe Laborinfrastruktur und geschultes Personal, was ihren Einsatz in vielen Regionen erschwert. Daher ist die Entwicklung von patientennahen Diagnoseverfahren von großer Bedeutung.
Der im Oktober 2025 in Trends in Biotechnology veröffentlichte Übersichtsartikel wurde von Dr. Defne Yi?ci von der Medizinischen Fakultät der Koç-Universität, Prof. Dr. Önder Ergönül vom ??bank-Zentrum für Infektionskrankheiten der Koç-Universität und der Abteilung für Infektionskrankheiten und Klinische Mikrobiologie der Medizinischen Fakultät der Koç-Universität sowie Prof. Dr. Sava? Ta?o?lu vom Institut für Maschinenbau und dem Translationalen Medizinforschungszentrum der Koç-Universität (KUTTAM) verfasst. Der Artikel untersucht umfassend patientennahe Diagnoseplattformen für die Mycoplasma-pox-Diagnostik, die zugrunde liegenden technischen Ansätze und die Hindernisse für deren breite Anwendung. Darüber hinaus werden zukünftige Entwicklungsrichtungen diskutiert, die die Integration molekularer Diagnostik mit KI- und Deep-Learning-basierten Werkzeugen umfassen.
Der erste Fall von Mycoplasma-Pocken beim Menschen wurde 1970 in der Demokratischen Republik Kongo gemeldet. Das Virus war zuvor in einer Makakenart nachgewiesen worden, die aus Afrika nach Dänemark eingeschleppt worden war. Das Mycoplasma-Pockenvirus kommt in Primaten, Eichhörnchen, Nagetieren und Präriehunden vor. Die Übertragung auf den Menschen erfolgt typischerweise durch Bisse oder Kratzer infizierter Tiere. Die Übertragung von Mensch zu Mensch kann durch engen Kontakt, Tröpfcheninfektion, Kontakt mit infektiösen Läsionen oder Körperflüssigkeiten erfolgen. Viele Jahre lang blieb die Krankheit weitgehend auf Zentral- und Westafrika beschränkt. Im Jahr 2003 wurden jedoch Fälle in den Vereinigten Staaten gemeldet. 2022 kam es zu einem weltweiten Ausbruch mit über 60.000 gemeldeten Fällen in mehr als 100 Ländern – die meisten davon galten zuvor nicht als Endemiegebiete.
Die Masernpocken beginnen meist mit unspezifischen Symptomen. In den ersten Tagen können Fieber, Muskelschmerzen, Kopfschmerzen und grippeähnliche Beschwerden auftreten. Darauf folgen oft schmerzhafte Lymphknotenschwellungen und Hautausschläge. Diese zeigen sich zunächst als kleine Flecken, erhaben sich dann, entwickeln sich zu mit Flüssigkeit gefüllten Bläschen und schließlich zu eitergefüllten Läsionen. Da dieses Krankheitsbild Masern, Windpocken, Syphilis und anderen Pockenvirusinfektionen ähneln kann, ist eine eindeutige Diagnose allein anhand der Symptome schwierig.
Die derzeit zuverlässigste Diagnosemethode ist der PCR-Test. Dabei wird das genetische Material des Virus in Proben von Hautläsionen nachgewiesen. Die PCR liefert hochsensitive und genaue Ergebnisse. Sie erfordert jedoch spezielle Geräte, Laborbedingungen und geschultes Personal. Daher ist die Anwendung direkt beim Patienten nicht immer möglich.
Die Forscher erörtern auch immunologische Tests zur Diagnose von Mycoplasma-pocken (Mpox). Serologische Tests wie ELISA finden in der klinischen Praxis nur begrenzt Anwendung. Da das Mpoxvirus Ähnlichkeiten mit anderen Viren derselben Familie aufweist, können falsch-positive Ergebnisse auftreten. Dies betrifft insbesondere Personen, die bereits gegen Pocken geimpft wurden. In den letzten Jahren wurden Antigen-Schnelltests entwickelt, die auf spezifische Virusproteine ??abzielen. Einige dieser Tests liefern Ergebnisse innerhalb von 10–15 Minuten. Sie sind jedoch im Allgemeinen weniger sensitiv als die PCR und können die Viruslast nur begrenzt quantifizieren. Fortschrittlichere Biosensorsysteme befinden sich in der Entwicklung, werden aber noch nicht flächendeckend eingesetzt.
Zu den Alternativen zur PCR zählen LAMP- und RPA-Verfahren. Diese Methoden arbeiten bei konstanter Temperatur und benötigen keine komplexe Thermocycler-Ausrüstung. In einigen Studien wurde eine vergleichbare Sensitivität wie bei der PCR festgestellt. Allerdings können sie gelegentlich falsch-positive Ergebnisse liefern und weisen begrenzte Multiplexing-Kapazitäten auf.
In den letzten Jahren findet die CRISPR/Cas-Technologie auch in der Diagnostik Anwendung. Diese Systeme können virales genetisches Material mit hoher Spezifität erkennen. In Kombination mit LAMP oder RPA erreichen sie eine sehr hohe Sensitivität. Zudem bieten sie das Potenzial, zwischen verschiedenen Mpox-Subtypen zu differenzieren. Verschiedene Ansätze zielen darauf ab, Reaktionen in einem einzigen Reaktionsgefäß und die Integration in tragbare Geräte zu ermöglichen. Kosten, technische Komplexität und die Notwendigkeit der Kühlkette für bestimmte Reagenzien stellen jedoch weiterhin wichtige Einschränkungen dar.
Ein weiterer wichtiger Punkt der Studie betrifft die Eigenschaften eines idealen patientennahen Diagnosetests. Laut WHO sollten solche Tests kostengünstig, zuverlässig, schnell, benutzerfreundlich, robust und leicht zugänglich sein. Diese Kriterien wurden später im Rahmen des „REASSURED“-Konzepts um Echtzeit-Konnektivität und einfache Probenentnahme erweitert. Aktuelle Technologien erfüllen in der Regel einige, aber nicht alle dieser Anforderungen gleichzeitig.
Zu den vielversprechenden zukünftigen Entwicklungsrichtungen zählen elektrochemische Biosensoren, papierbasierte Tests und mikrofluidische Chipsysteme. Additive Fertigung mittels 3D-Druck und die Integration in Smartphones können dazu beitragen, Kosten zu senken und die Skalierbarkeit zu verbessern. Darüber hinaus können KI-basierte Systeme Bilder von Hautläsionen zur ersten Beurteilung analysieren. Obwohl solche Instrumente molekulare Tests nicht ersetzen sollen, können sie insbesondere in Gebieten mit wenigen Fachärzten als nützliche Screening-Methoden dienen.
Zusammenfassend lässt sich sagen, dass die PCR zwar weiterhin der Goldstandard für die Mpox-Diagnostik ist, der Bedarf an schnellen und leicht zugänglichen Diagnoseverfahren jedoch insbesondere in ressourcenarmen Umgebungen stetig wächst. Technologien wie LAMP, RPA und CRISPR bergen großes Potenzial, diese Lücke zu schließen. Herausforderungen in Bezug auf Kosten, Massenproduktion, Feldanwendbarkeit und Integration in Gesundheitssysteme müssen jedoch noch bewältigt werden. Die Zukunft liegt wahrscheinlich in integrierten Diagnoseplattformen, die molekulare Tests, Biosensortechnologien und KI-gestützte Entscheidungssysteme kombinieren.
https://doi.org/10.1016/j.tibtech.2025.04.015.