Viren sind Meister darin, in unsere Zellen einzudringen, dank spezialisierter Proteine ??auf ihrer Oberfläche. Bei der Entwicklung von Impfstoffen stellen Wissenschaftler häufig Varianten dieser viralen Oberflächenproteine ??her, um die Reaktion unseres Immunsystems zu untersuchen. Doch diesen im Labor hergestellten Proteinen fehlen typischerweise wichtige Bestandteile der Virusmembran, weshalb sie sich nicht immer so verhalten wie auf einem echten Virus. Dies erschwerte bisher das Verständnis, wie Antikörper diese viralen Zielstrukturen erkennen und neutralisieren.
Wissenschaftler des Scripps Research Institute haben nun in Zusammenarbeit mit IAVI und anderen Instituten eine Plattform entwickelt, die es ermöglicht, virale Oberflächenproteine ??in einer Form zu untersuchen, die ihrem natürlichen Erscheinungsbild deutlich ähnlicher ist. Der neue Ansatz nutzt die Nanodisc-Technologie, bei der diese Proteine ??in Partikel aus Lipidmolekülen eingebettet und so in einer membranähnlichen Struktur erhalten werden. Dies könnte die Impfstoffforschung voranbringen, indem es die Interaktion zwischen Antikörpern und viralen Proteinen besser aufklärt.
Die Plattform, die am 10. Februar 2026 in Nature Communications vorgestellt wurde , wurde anhand von Proteinen von HIV und Ebola getestet: zwei Viren, die Impfstoffentwickler seit Langem vor Herausforderungen stellen, da ihre Oberflächenproteine ??für das Immunsystem schwer zu erkennen sind. Der Ansatz könnte jedoch auch auf andere Viren mit ähnlichen Membranproteinen, wie beispielsweise Influenza und SARS-CoV-2, angewendet werden.
„Viele Jahre lang waren wir auf Varianten viraler Proteine ??angewiesen, denen wichtige Teile fehlten“, sagt William Schief , Professor am Scripps Research Institute und Leiter der Impfstoffentwicklung am Neutralizing Antibody Center des IAVI. „Unsere Plattform ermöglicht es uns, diese Proteine ??in einer Umgebung zu untersuchen, die ihre natürliche Umgebung besser widerspiegelt. Dies ist entscheidend, um zu verstehen, wie schützende Antikörper ein Virus erkennen.“
Bei echten Viren liegen Oberflächenproteine ??nicht frei vor, sondern sind in eine Lipidmembran eingebettet und in spezifischen Formen angeordnet. In den meisten Laborstudien wird jedoch die Membranverankerung entfernt, um die Proteine ??einfacher herzustellen und zu analysieren. Diese Vereinfachungen sind zwar nützlich, können aber wichtige Merkmale verschleiern, insbesondere bei Antikörpern, die Regionen nahe der Proteinbasis, also in der Nähe der Virusmembran, angreifen.
Um dieses Problem zu lösen, hat das Forschungsteam virale Proteine ??von Impfstoffkandidaten in Nanodiscs eingebettet. Nanodiscs sind kleine, stabile Membranfragmente, die die Proteine ??fixieren. Diese Lipiddiscs ahmen die äußere Schicht des Virus nach und tragen so dazu bei, dass die Erkennung von Proteinen durch Antikörper in einem echten Virus erhalten bleibt. Ihre neuartige Plattform ermöglichte es den Forschern, eine Reihe gängiger Methoden der Impfstoffentwicklung anzuwenden, darunter Tests zur Antikörperbindung, die Sortierung von Immunzellen und hochauflösende Bildgebung.
„Die Integration all dieser Komponenten in ein einziges, zuverlässiges System war der Schlüssel“, erklärt Erstautor Kimmo Rantalainen, leitender Wissenschaftler in Schiefs Labor. „Die einzelnen Bausteine ??existierten bereits, aber ihre reproduzierbare und skalierbare Funktionsweise eröffnet neue Möglichkeiten für die Analyse und Entwicklung von Impfstoffen.“
Am Beispiel von HIV konzentrierte sich das Team auf eine konservierte Region des Oberflächenproteins des Virus, die sich nahe der Membran befindet. Diese Region wird von einer Klasse von Antikörpern angegriffen, die nahezu alle HIV-Varianten blockieren können. Solche Antikörper erkennen virale Bestandteile, die auch bei Mutationen ähnlich bleiben – eine Immunantwort, die Wissenschaftler hoffen, dass Impfstoffe zukünftig auslösen können.
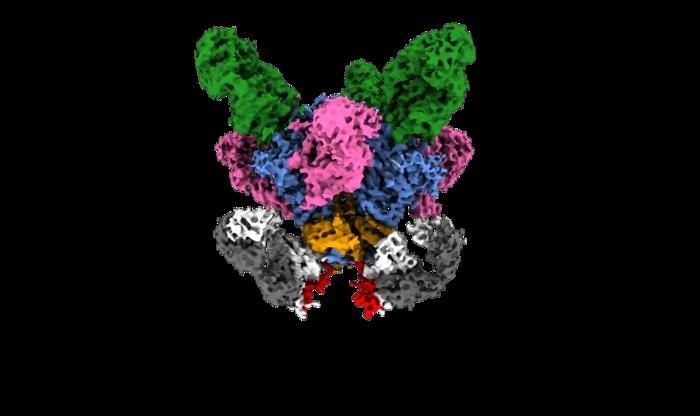
Mithilfe ihrer Nanodisc-Plattform konnten die Forscher detaillierte Strukturaufnahmen der Interaktion von Antikörpern mit viralen Proteinen in deren Membrankontext erstellen. Dabei wurden Merkmale sichtbar, die bei der Untersuchung des Proteins allein nicht erkennbar sind. Diese Erkenntnisse tragen auch dazu bei, zu erklären, wie bestimmte Antikörper ein Virus neutralisieren können, indem sie die Proteinstrukturen destabilisieren, die es zur Infektion von Zellen nutzt. Dies liefert Hinweise darauf, wie zukünftige Impfstoffe ähnliche Immunreaktionen besser auslösen könnten.
„Die Struktur ermöglichte uns einen Detailgrad, der uns zuvor schlichtweg nicht zugänglich war“, erklärt Rantalainen. „Sie zeigte uns neue Interaktionen an der Membranoberfläche und verdeutlichte, warum diese für die Antikörperfunktion relevant sind.“
Credits: Scripps Research